Células madres y cáncer: atracción fatal?
INTRUCCIÓN
Las investigaciones que se están llevando a cabo con células madre, o stem cells, están abriendo nuevas estrategias para combatir los tumores malignos. En líneas generales, las stem cells son un tipo de células que tienen la virtud natural de poder convertirse en cualquiera de las variedades celulares que integran nuestro organismo. Las células madre normales y las cancerígenas comparten la capacidad de su propia regeneración. Por eso, parece lógico proponer que las nuevas células cancerígenas adaptan su maquinaria para llevar a cabo una división de autorregeneración similar a la que expresan las células madre. En la mayor parte de las neoplasias, se desconoce cuál es el objetivo celular de la trasformación de las mutaciones. Sin embargo, existe información contundente de que ciertas formas de leucemia se desarrollan a partir de las mutaciones que se acumulan en las células madre hematopoyéticas.
Por otra parte, si el crecimiento tumoral y metastásico se conduce por una pequeña población de células madre cancerígenas, podría explicar los errores en el desarrollo de terapias que sean capaces de erradicar los tumores sólidos. Aunque los fármacos existentes pueden reducir el tamaño de los tumores metastásicos, esos efectos son normalmente transitorios y en ocasiones no se reflejan en un aumento de la vida del paciente. Una razón del fallo de estos tratamientos es la resistencia a quimioterápicos que aparecen en estas células. Otra posibilidad de los fracasos terapéuticos es que fallen los tratamientos dirigidos a destruir las células madre cancerígenas.
En la mayoría de las neoplasias existen células madre cancerígenas que se pueden auto-regenerar de forma indefinida, en contraste con las células madre que pueden tener un potencial proliferativo limitado. Por eso, para curar el cáncer es necesario poder destruir las células madre cancerígenas y caracterizar e identificar sus propiedades.
CÉLULAS MADRE, PERO COMO CAUSA DE TUMORES
Profundizar y comprender mejor la biología normal ha puesto en evidencia que las células madres tienen un rol principal no sólo en la organización de seres multicelulares complejos sino también en el desarrollo de tumores, siendo su acción principal el aumento y perpetuación de muchas formas de cáncer humano. La erradicación de estas unidades de un tumor también puede ser esencial para alcanzar la remisión estable, duradera, e incluso una curación del cáncer. En este artículo se analizan las propiedades de las células madres cancerosas, se delinean estrategias terapéuticas iniciales en su contra y se establecen desafíos a futuro.
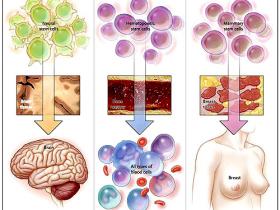
Las células madres se observan en diferentes tejidos somáticos y son piezas importantes en su fisiología (figura 1). La población de estas células se organiza en forma jerárquica con la célula madre en su vértice (figura 2).

A: sistema nervioso central. B: sistema hematopoyético. C: tejido mamario.
Tienen tres propiedades distintivas: son auto-renovables, o sea al dividirse las dos células hijas tienen las mismas propiedades que la madre. Poseen la capacidad de desarrollar múltiples linajes y por último, el potencial de proliferar en forma extensiva. Estas tres características las hacen únicas y su potencial las acerca a lo que se denomina el fenotipo maligno. De acuerdo a lo anterior, las células que inician un tumor llevan las tres propiedades y es así como se les llama células madres cancerosas (figura 2).

El tejido normal proviene de células madres centrales que crecen y se diferencian para crear las células progenitoras y luego la población de células maduras. Las propiedades de las células madres es su auto-reproducción (flecha curva), potencialidad de producir múltiples linajes (flechas) y capacidad de seguir multiplicándose. La unidad madre cancerosa es una mutación en las células madre o progenitoras. Éstas se pueden reproducir produciendo poblaciones heterogéneas de células hijas y proliferar extensivamente.
Las stem cells cancerosas son mutaciones de las células madres normales, pero también pueden provenir de las células progenitoras las que deben mutar y adquirir la capacidad de auto-renovación. Un pequeño grupo de estas células es esencial en un tumor maligno. Ellas pueden ser el origen de todas las unidades que componen un tumor y pueden ser la reserva quimio-resistente, las que producen recidivas o metástasis a distancia (figura 3).

A: mutación de una célula madre o progenitora normal. B: destrucción de las células tumorales con quimioterapia pero persistencia de las células madre y recidiva del tumor. C: migración de células madres y producción de metástasis.
Es evidente que un tratamiento que destruyó un tumor y que posteriormente recidivó, se debe a las células madres tumorales que no fueron eliminadas (figura 3-b).
El sistema hematopoyético es el mejor tejido para el estudio de las células madres. En muchas leucemias las células madres han sido identificadas igualmente que sus propiedades biológicas. Son fácilmente evidenciables en la leucemia mielocítica crónica (LMC), en la leucemia mielocítica aguda (LMA) y el la leucemia linfoblástica (LLA). Las células madres de la LMA tienen marcadores superficiales como la interleuquina 3-receptor alfa que no está presente en las células madres normales, lo que las hace accequibles a tratamientos basados en anticuerpos por lo que se estudian reacciones inmunoterapéuticas en su contra.
Se han estudiado extensamente drogas que específicamente modulan los pasos en el crecimiento de las células leucémicas. Es así como el imatinib, un inhibidor de la proteína tirosina quinasa ABL, se ha demostrado importante en el tratamiento de la LMC.
Los estudios in vitro han demostrado que la inhibición del producto translocado BCR-ABL de la LMC es suficiente para eliminar la mayoría de las células leucémicas, pero aparentemente no elimina las células madres de la LMC. El imatinib afecta la progenia de las células madres pero no éstas mismas por lo que la enfermedad recurre si se discontinúa el tratamiento. Sin embargo, hay evidencias que algunos factores nucleares como el NH-kB y la Fosfatidilinositol 3 (PL3 quinasa) son señales de comunicación de las células madres de la LMC y no se encuentran en las células madres normales por lo que podría usarse como blanco específico para atacarlas, lo que de hecho se ha logrado in vitro sin alteración de las células madres normales. Algo semejante se ha conseguido en el paso del PL3 en leucemias inducidas en ratas lo que hace pensar que por este camino se puede llegar a tratar las células madres leucémicas.
A nivel del sistema nervioso central (SNC) también se ha logrado obtener células madres. Ya en 1992 se había descubierto que el cultivo de células del SNC en superficies no adherentes producía bolas de células llamadas “neuroesferas” con capacidad de auto-reproducción y que pueden producir cualquier tipo de células cerebrales (neuronas, astrositos, ologodendrocitos, etc). Si se saca una pequeña porción de esta neuroesfera, se reproduce otra igual a la originaria (figura 4). Últimamente se ha demostrado que las células madres cerebrales tienen una proteína de superficie que puede ser detectada con un anticuerpo, el AC133 (CD133) epítope, un marcador encontrado comúnmente en células madres o progenitoras de varios tejidos.

Si se aíslan las células madres del SNC y se transplantan unas 100 CD 133, células de glioma humano positivas, en cerebros de ratas inmunodeprimidas se observa la obtención de gliomas, en cambio no sucede esto si los CD 133 son negativos, aunque el número de implantados sea un millón de células. Por otra parte se ha demostrado que también se pueden obtener tumores de células progenitoras siempre que estas hayan obtenido las propiedades de una célula madre. Desde el punto de vista terapéutico el que se puedan cultivar células madres o progenitoras nos permiten suponer que estudios hechos sobre ellas nos lleven a encontrar medicamentos que las destruyan o eliminen.
Otro tumor en que se ha demostrado fehacientemente la importancia de las stem cells es el carcinoma de la mama. Células con un antígeno de superficie tipo CD44 positivo o CD24 negativo, pueden reproducirse al transplantarse en ratas inmunodeprimidas. La distinción de las células madres cancerosas y normales ha avanzado rápidamente. Ya se han podido estudiar células madres de mama las que han reproducido experimentalmente una glándula mamaria. El estudio de las células de tipo canceroso está en marcha. Ahora los desafíos que tenemos para el tratamiento del cáncer es conocer más sobre las características de las células madre cancerosas, porque los tratamientos que destruyen una masa tumoral dejan indemne estas células que parecen ser las causas de las recidivas.
Otro desafío, es por qué estas células son tan difíciles de eliminar. Al menos en las células madres de la leucemia se ve que estas pasan casi permanentemente en estado latente y por lo tanto inmunes a los quimioterápicos. Por lo tanto, se tendrá que buscar agentes que actúen fuera del ciclo celular o específicamente en su ciclo. Otras características de estas células es la expresión de proteínas asociadas al flujo de toxinas xenobióticas (o sea multiresistentes).
Las células madres anormales (cancerosas) han perdido la capacidad natural de producir apoptósis como lo hacen las células madres normales cuando se ha alterado su ADN. Por esto mismo pueden ser más resistentes a la acción de los quimioterápicos. Al contrario, como se ha visto en células madres del sistema hematopoyético que van a la “senescencia” cuando son alteradas por medicamentos o radiaciones ionizantes, las células madres cancerosas aprovechan mejor el mayor espacio disponible para reproducirse ventajosamente. De ahí la importancia de saber como detectar los nidos madres cancerosos residuales después de una terapia.
Es importante saber los pasos que controlan las reacciones de las stem cells tumorales. Pero aún así conocidas estas etapas no sabemos si los tratamientos eliminan las células madres cancerosas o sólo detienen su evolución. Por eso debemos conocer los pasos seguidos por ellas para la supervivencia. Aquí habría que estudiar las bases oxidativas o las terapias basadas en anticuerpos o en los ligantes de bases. Estos estudios nos llevarán a demostrar si ellos u otros medios pueden distinguir entre las células madres cancerosas y los tejidos normales.
Fuente bibliográfica
Cancer stem cells
Craig T. Jordan, Ph.D., Monica L. Guzman, Ph.D., and Mark Noble, Ph.D.
James P. Wilmot Cancer Center, University of Rochester School of Medicine, Rochester, NY 14642, USA.
N Engl J Med. 2006 Sep 21;355(12):1253-61